2026年4月27日,广州国家实验室陈新文团队联合中国科学院广州生物医药与健康研究院、山东大学、中国科学院武汉病毒所、广州医科大学等单位的研究团队在学术期刊Cell上发表题为“Differential inhibition of Morbillivirus and Henipavirus polymerases by ERDRP-0519 and structure-guided inhibitor optimization”研究论文,系统解析了小分子抑制剂ERDRP-0519在麻疹病毒属以及亨尼帕病毒属病毒聚合酶中的作用机制,并基于结构与功能信息对抑制剂进行优化设计。本研究整合冷冻电镜结构解析获得了抗病毒活性更优的新型候选分子GL22和G671,为高致病性副黏病毒广谱药物研发提供关键理论基础与全新候选化合物。
副黏病毒目包含多种重要人类及动物病原体,如麻疹病毒、小反刍兽疫病毒及尼帕病毒等。其中,尼帕病毒具有较高致死率和跨种传播能力,被世界卫生组织列为重点关注的新发传染病病原之一。然而,目前全球仍缺乏针对尼帕病毒感染的特异性抗病毒药物,因此,靶向病毒复制酶的药物研发具有重要科学价值与现实需求。
研究团队发现,最初针对麻疹病毒开发的小分子抑制剂ERDRP-0519,除对麻疹病毒及小反刍兽疫病毒等麻疹病毒属成员具有较强抑制作用外,还可对亨尼帕病毒属的尼帕病毒产生交叉抑制作用。通过整合冷冻电镜结构解析、生化细胞实验与病毒学功能验证,团队揭示ERDRP-0519能够结合于麻疹病毒、小反刍兽疫病毒以及尼帕病毒RNA依赖的RNA聚合酶(RdRp)手掌结构域中的一个较为保守的结合口袋。ERDRP-0519通过占据这一关键位置,阻碍RNA模板和核苷酸结合聚合酶活性中心,从而抑制病毒RNA的合成。
本研究还首次揭示,相较于与麻疹病毒属聚合酶的结合,ERDRP-0519在结合尼帕病毒聚合酶时需要诱导其结合口袋发生更明显的构象变化,因而可能伴随更高的能量代价进而导致结合亲和力下降,这在一定程度上解释了其对尼帕病毒抑制作用相对较弱的现象。
在上述机制基础上,研究团队进一步对ERDRP-0519进行定向优化,获得了两种衍生物GL22和G671。两种新化合物通过引入延伸基团介导跨结构域相互作用,增强了与尼帕病毒聚合酶的结合,同时增加了对RNA模板及核苷酸结合的空间位阻,从而提升了对尼帕病毒聚合酶的抑制活性。
综上,本研究系统阐明了ERDRP-0519跨属抑制副黏病毒聚合酶的分子基础,揭示了相对保守的聚合酶药物结合口袋在不同病毒中的精细结构差异及其抗病毒的影响,提出了针对该口袋跨病毒差异进行精准优化的药物设计策略,相关成果不仅为开发针对尼帕病毒等高致病性病毒的聚合酶抑制剂提供了新的候选化合物和设计思路,也为广谱抗副黏病毒药物研发提供了基础。
副黏病毒目包含多种重要人类及动物病原体,如麻疹病毒、小反刍兽疫病毒及尼帕病毒等。其中,尼帕病毒具有较高致死率和跨种传播能力,被世界卫生组织列为重点关注的新发传染病病原之一。然而,目前全球仍缺乏针对尼帕病毒感染的特异性抗病毒药物,因此,靶向病毒复制酶的药物研发具有重要科学价值与现实需求。
研究团队发现,最初针对麻疹病毒开发的小分子抑制剂ERDRP-0519,除对麻疹病毒及小反刍兽疫病毒等麻疹病毒属成员具有较强抑制作用外,还可对亨尼帕病毒属的尼帕病毒产生交叉抑制作用。通过整合冷冻电镜结构解析、生化细胞实验与病毒学功能验证,团队揭示ERDRP-0519能够结合于麻疹病毒、小反刍兽疫病毒以及尼帕病毒RNA依赖的RNA聚合酶(RdRp)手掌结构域中的一个较为保守的结合口袋。ERDRP-0519通过占据这一关键位置,阻碍RNA模板和核苷酸结合聚合酶活性中心,从而抑制病毒RNA的合成。
本研究还首次揭示,相较于与麻疹病毒属聚合酶的结合,ERDRP-0519在结合尼帕病毒聚合酶时需要诱导其结合口袋发生更明显的构象变化,因而可能伴随更高的能量代价进而导致结合亲和力下降,这在一定程度上解释了其对尼帕病毒抑制作用相对较弱的现象。
在上述机制基础上,研究团队进一步对ERDRP-0519进行定向优化,获得了两种衍生物GL22和G671。两种新化合物通过引入延伸基团介导跨结构域相互作用,增强了与尼帕病毒聚合酶的结合,同时增加了对RNA模板及核苷酸结合的空间位阻,从而提升了对尼帕病毒聚合酶的抑制活性。
综上,本研究系统阐明了ERDRP-0519跨属抑制副黏病毒聚合酶的分子基础,揭示了相对保守的聚合酶药物结合口袋在不同病毒中的精细结构差异及其抗病毒的影响,提出了针对该口袋跨病毒差异进行精准优化的药物设计策略,相关成果不仅为开发针对尼帕病毒等高致病性病毒的聚合酶抑制剂提供了新的候选化合物和设计思路,也为广谱抗副黏病毒药物研发提供了基础。

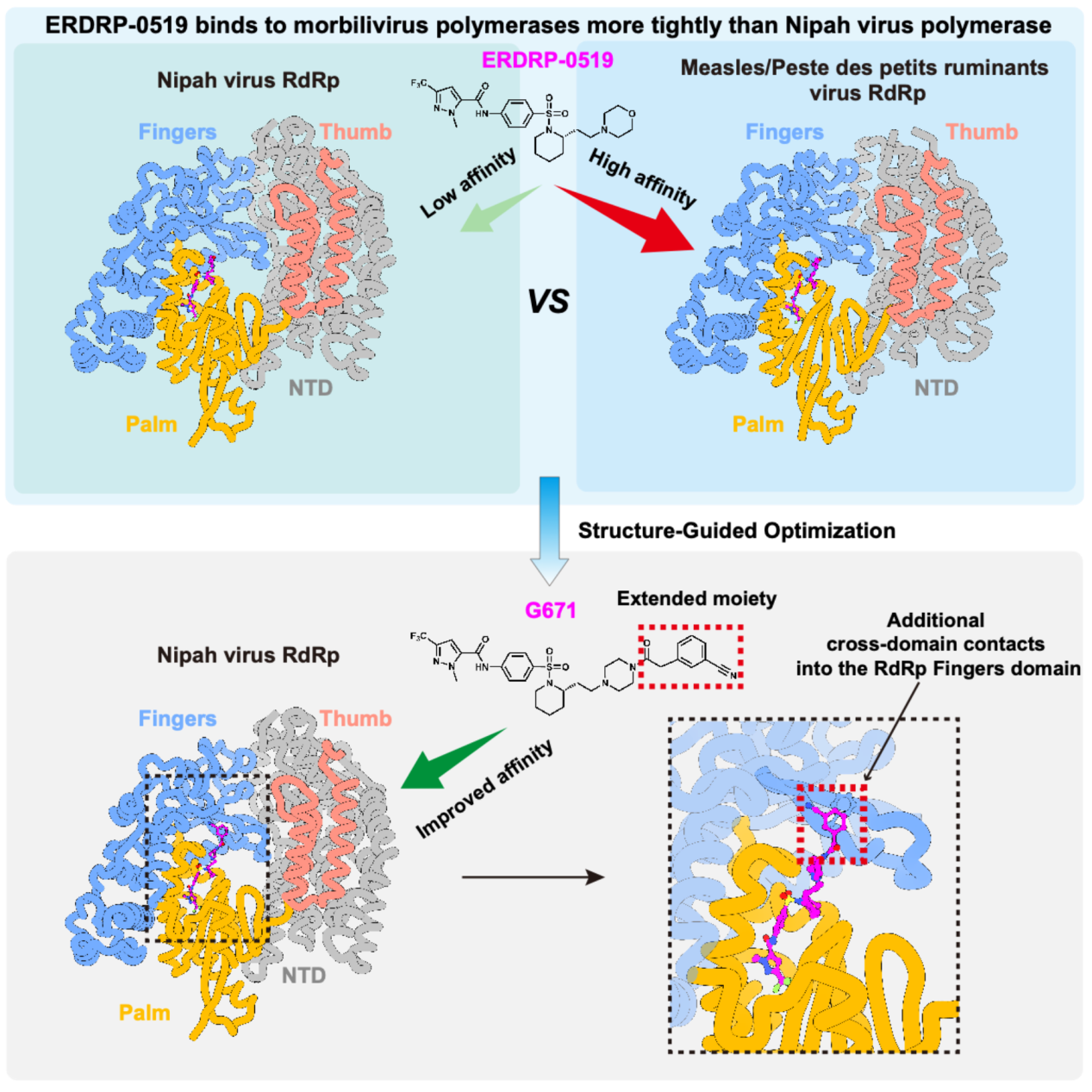
图1 ERDRP-0519对麻疹病毒属聚合酶的结合亲和力高于尼帕病毒聚合酶,其优化衍生物G671通过理性设计的化学骨架延伸形成额外跨结构域相互作用,提升了对尼帕病毒聚合酶的结合能力
广州国家实验室陈新文研究员,中国科学院广州生物医药与健康研究院熊晓犁研究员、何俊研究员,山东大学展鹏教授,中国科学院武汉病毒所裴荣娟研究员为本文的共同通讯作者。本研究受到伊利诺伊大学芝加哥分校荣立军教授,ERDRP-0519分子发明人美国乔治亚州立大学生物医学研究所Richard K. Plemper教授等的鼎力合作支持。
论文链接:https://www.cell.com/cell/abstract/S0092-8674(26)00400-9






