2026年1月28日,广州国家实验室范小英团队在Clinical and Translational Medicine杂志上发表了题“High-throughput single-cell DNA methylation and chromatin accessibility co-profiling with SpliCOOL-seq”的研究论文,开发出一种名为SpliCOOL-seq的高通量单细胞多组学测序技术(图1)。该技术突破性实现数千个细胞的全基因组DNA甲基化和染色质可及性同步精准测量分析,为解析肺腺癌等呼吸系统恶性肿瘤的表观遗传调控机制、推动精准诊疗提供了全新工具。
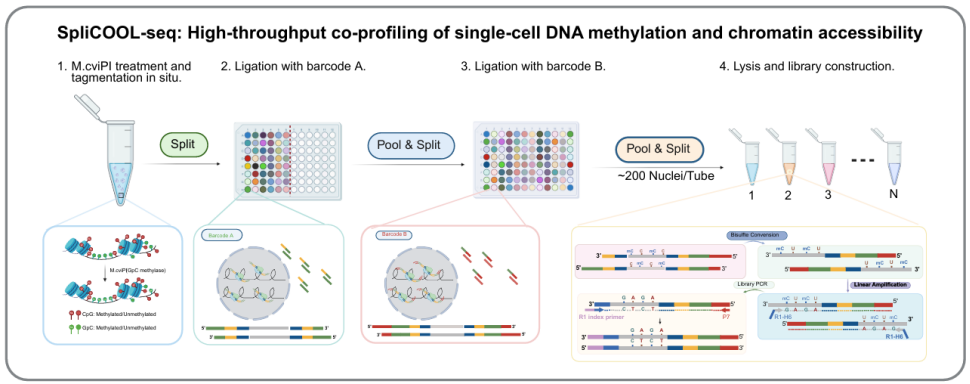
图1 SpliCOOL-seq流程
作为全球发病率和死亡率最高的恶性肿瘤之一,肺癌(尤其是肺腺癌)的异质性强、演化机制复杂,一直是临床诊疗的重点与难点。表观遗传调控紊乱是肿瘤发生发展的核心驱动力,其中DNA甲基化与染色质可及性的协同作用失衡,在肺腺癌的恶性转化中扮演关键角色。然而,传统单细胞测序技术(scCOOL-seq、scNMT-seq等)依赖细胞裂解液,存在通量低、成本高、耗时久等瓶颈,难以规模化解析肿瘤微环境中复杂的表观遗传异质性,极大限制了对肺腺癌发病机制的深度探究。
针对这一技术痛点,广州国家实验室范小英团队立足呼吸疾病研究前沿需求,整合原位GpC甲基化标记、通用Tn5标签化及组合条形码技术,成功构建SpliCOOL-seq技术体系。该技术首次实现对数千个细胞的全基因组DNA甲基化与染色质可及性的同步高通量分析,不仅具备更高的灵敏度与可扩展性,还能精准捕获核小体缺失区域(NDR)及拷贝数变异(CNV),为单细胞层面解析表观遗传协同调控规律提供了强大工具。在A549、H460、SK-MES等肺癌细胞系验证发现,该技术可清晰区分不同细胞类型的表观遗传特征,与现有scATAC-seq数据高度吻合,证实了其高精准度与可靠性。
依托SpliCOOL-seq技术,研究团队在肺腺癌表观遗传研究中取得系列创新性发现。
1.揭示DNMT抑制剂作用新模式。研究发现5-氮杂胞苷和地西他滨两种临床常用去甲基化药物的作用模式存在显著差异,靶向区域各有偏好,为肺腺癌临床个体化用药提供了科学依据。
2.发现肺腺癌肿瘤内亚克隆。首次在单细胞层面揭示肺腺癌肿瘤组织内存在不同拷贝数变异和表观遗传特征的亚克隆,还识别出一组“癌旁癌变细胞”(AC)——这类细胞已出现基因组异常但表观遗传状态接近正常,为理解肺腺癌早期演化轨迹、开发早期干预策略提供了全新视角。
3.鉴定新型预后相关甲基化标志物。发现一批与肺癌患者生存相关的新型DNA甲基化生物标志物标志基因(如FAM124B、SFN、OR7E47P)并通过CRISPR基因敲除和功能实验验证了SFN基因在促进肺癌细胞增殖和迁移中的关键作用。
4.揭示癌细胞表观遗传“加速衰老”。首次在单细胞层面发现,肿瘤细胞表现出明显的表观遗传年龄加速和细胞分裂速率加快,且与正常细胞共享部分衰老相关的甲基化信号,提示衰老与肿瘤发生存在共同的表观遗传基础。为肿瘤发生提供了新的见解。
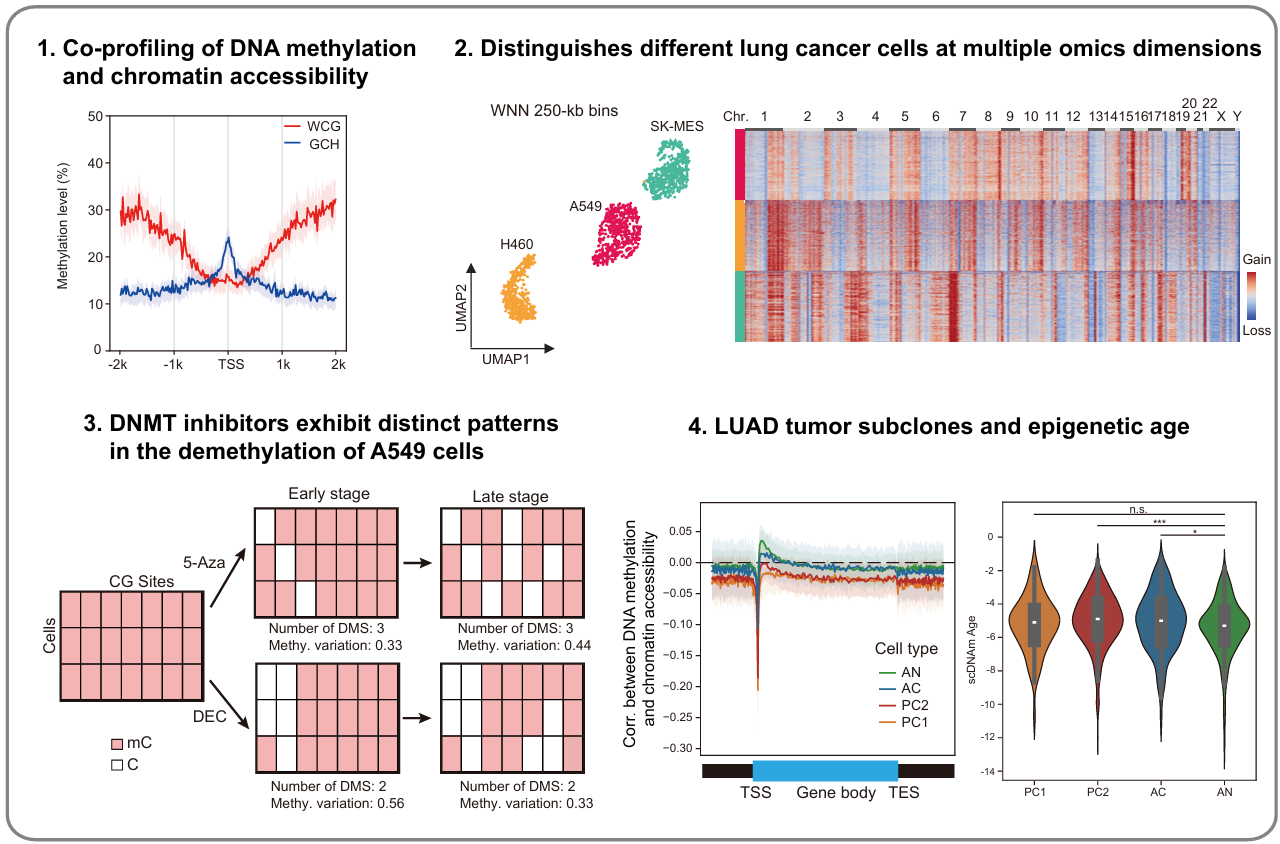
图2 SpliCOOL-seq解析肺癌细胞表观异质性及表观衰老
综上所述,本研究开发出一种高通量单细胞测序技术SpliCOOL-seq,可在单个细胞内同步完成全基因组DNA甲基化与染色质可及性的平行分析。该集成分析方法能够开展高分辨率、多模态的单细胞表观遗传学研究,在解析不同细胞状态下基因调控的相互作用机制方面展现出巨大潜力,同时也为癌症生物标志物的筛选搭建了强大的技术平台。相关应用研究已成功挖掘出全新的治疗靶点与早期诊断标志物,进一步凸显了这项技术在精准肿瘤学领域的重要应用价值。
论文链接:http://dx.doi.org/10.1002/ctm2.70584






