慢性阻塞性肺病(chronic obstructive pulmonary disease,COPD)是全球第三大死因,也是当前全球公共卫生领域面临的重大挑战之一。吸烟是COPD最重要的危险因素,长期烟草烟雾暴露可导致肺功能持续下降、肺组织结构破坏及慢性炎症反应。然而,吸烟诱导的COPD背后具体的免疫学机制仍未完全阐明,尤其是肺组织及循环系统中T细胞在烟雾刺激下如何发生重塑、迁移和功能转变,仍缺乏系统性的认知。
2025年12月,广州医科大学附属第一医院/广州国家实验室冉丕鑫教授、王忠芳教授和周玉民教授团队在国际权威期刊Nature Communications(IF:15.7)发表研究论文“Comprehensive profiling of smoke-induced T cells in mice implicates clonal γδT17 cells as a hallmark of COPD”,通过多维度单细胞技术和功能学实验,系统描绘了烟雾相关的T细胞免疫图谱,并首次明确克隆化扩增的γδT17细胞在COPD发生发展中的关键作用。冉丕鑫教授、王忠芳教授与周玉民教授为本文共同通讯作者,梅馨月博士后、王俊翔副研究员、王媛博士及程莉为本文共同第一作者。
2025年12月,广州医科大学附属第一医院/广州国家实验室冉丕鑫教授、王忠芳教授和周玉民教授团队在国际权威期刊Nature Communications(IF:15.7)发表研究论文“Comprehensive profiling of smoke-induced T cells in mice implicates clonal γδT17 cells as a hallmark of COPD”,通过多维度单细胞技术和功能学实验,系统描绘了烟雾相关的T细胞免疫图谱,并首次明确克隆化扩增的γδT17细胞在COPD发生发展中的关键作用。冉丕鑫教授、王忠芳教授与周玉民教授为本文共同通讯作者,梅馨月博士后、王俊翔副研究员、王媛博士及程莉为本文共同第一作者。

图1 Nature Communications官方论文首页
烟雾暴露驱动T细胞空间分布重塑
研究团队首先聚焦于烟雾暴露后T细胞整体免疫格局的变化。通过创新性地结合静脉与鼻内免疫标记策略,分别区分血管内与气道表面的免疫细胞,系统比较了烟雾暴露2个月和6个月后T细胞在肺组织微环境及循环系统中的动态分布特征。
研究结果显示,烟雾暴露显著改变了T细胞的空间分布和迁移模式。与空气对照组相比,气道内T细胞数量明显增加,且在暴露2个月时最为显著;与此同时,血管内T细胞数量相应减少(图2)。这一现象提示,在烟雾刺激下,T细胞可能由循环系统被持续募集至气道区域,参与局部免疫应答和炎症反应。
研究结果显示,烟雾暴露显著改变了T细胞的空间分布和迁移模式。与空气对照组相比,气道内T细胞数量明显增加,且在暴露2个月时最为显著;与此同时,血管内T细胞数量相应减少(图2)。这一现象提示,在烟雾刺激下,T细胞可能由循环系统被持续募集至气道区域,参与局部免疫应答和炎症反应。
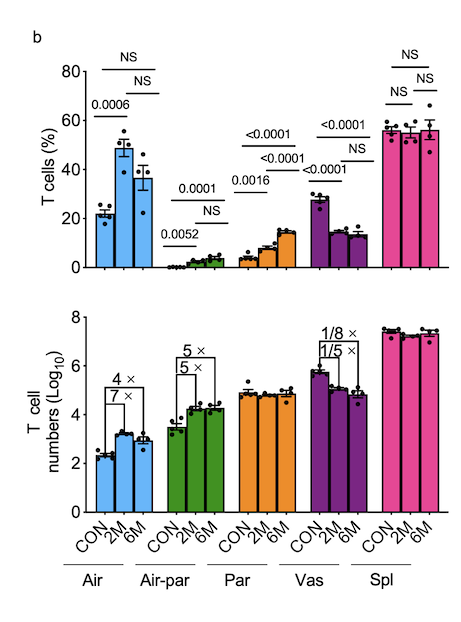
图2 烟雾暴露后小鼠不同组织部位的T细胞的比例和数量动态变化
进一步分析T细胞亚群组成发现,烟雾暴露后气道内CD4⁺ T细胞与CD8⁺ T细胞的占比均显著升高,而CD4⁻CD8⁻ T细胞的占比则呈下降趋势(图3)。上述发现提示,T细胞可能在COPD疾病进展中发挥重要作用,其中CD4⁻CD8⁻ T细胞比例的变化可能与COPD的发生发展相关。
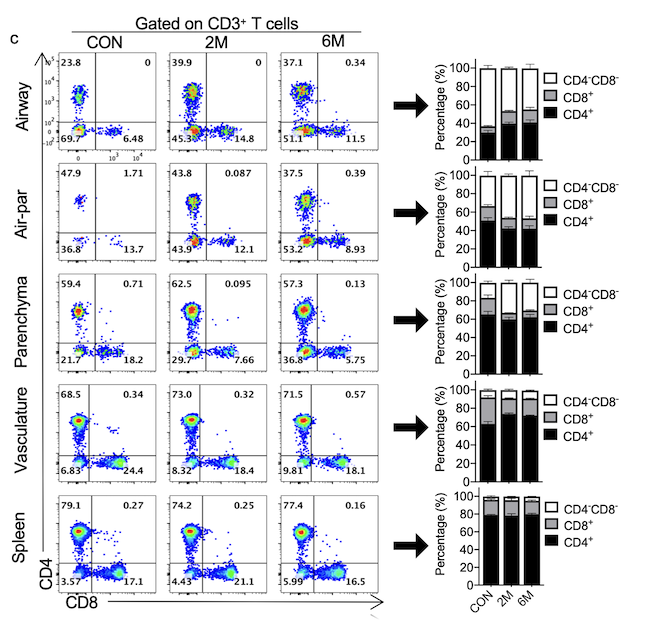
图3 烟雾暴露后小鼠不同组织部位的T细胞亚群分布
T细胞免疫系统在烟雾暴露下发生改变
为进一步探究烟草烟雾暴露后T细胞的亚群构成、细胞来源及功能作用,研究团队构建了烟草烟雾暴露2个月和6个月的动物模型,并利用单细胞转录组技术对肺组织中的T细胞进行系统刻画(图4a)。结果显示,烟雾暴露可显著重塑T细胞亚群比例,并引发其基因表达谱的广泛改变,提示烟雾刺激不仅影响T细胞数量分布,也深刻重编程其功能状态。
为进一步探究烟草烟雾暴露后T细胞的亚群构成、细胞来源及功能作用,研究团队构建了烟草烟雾暴露2个月和6个月的动物模型,并利用单细胞转录组技术对肺组织中的T细胞进行系统刻画(图4a)。结果显示,烟雾暴露可显著重塑T细胞亚群比例,并引发其基因表达谱的广泛改变,提示烟雾刺激不仅影响T细胞数量分布,也深刻重编程其功能状态。
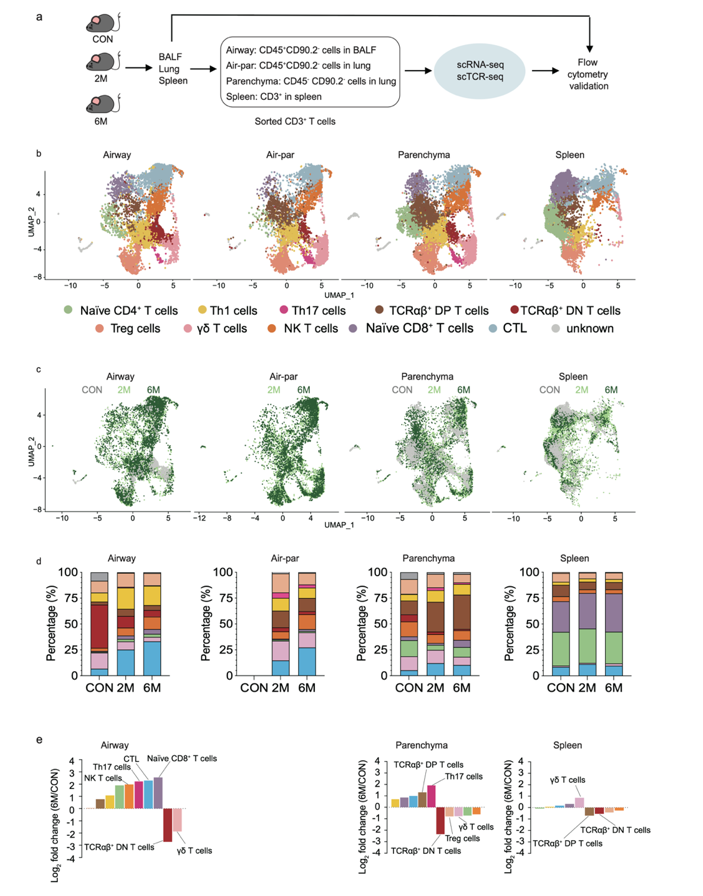
图4 烟雾暴露相关的小鼠T细胞单细胞图谱
TCR测序揭示气道T细胞抗原应答增强
为评估烟雾暴露后T细胞是否经历抗原驱动的克隆扩增,研究团队将单细胞靶向转录组与TCR测序相结合,对不同组织部位的T细胞克隆特征进行了系统分析。结果发现,烟雾暴露后,气道T细胞可能受到多种抗原的刺激,进而导致其TCR克隆的多样性与特异性增强。相比之下,γδT细胞则维持着相对稳定的克隆特征(图5),这一发现引起了研究者的进一步关注。
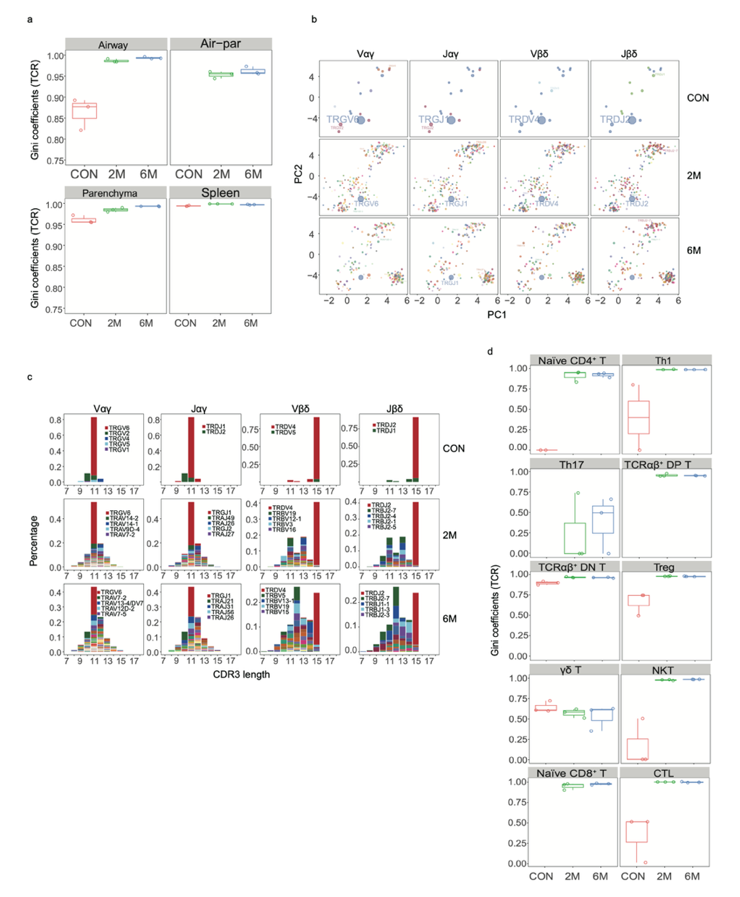
图5 烟雾暴露后小鼠气道上T细胞的TCR多样性增加
γδT细胞向γδT17表型分化并克隆扩增
γδT细胞是一类广泛分布于黏膜组织的先天样淋巴细胞,具有独特的抗原识别方式和快速应答能力,在炎症调控、免疫稳态维持和组织修复中发挥重要作用。研究团队发现,在烟雾暴露条件下,γδT细胞尽管在气道中的整体比例有所下降,但其内部组成和功能状态却发生了显著改变。
具体而言,烟雾暴露显著诱导γδT细胞高表达Il17a,并伴随着γ6δ4 T细胞这一优势克隆类型的明显扩增(图6a-d)。随着暴露时间延长,γ6δ4 T细胞持续发生克隆化扩增,并逐步获得典型的γδT17表型特征(图6e-g)。上述结果提示,克隆化扩增的γδT17细胞可能构成烟雾暴露相关免疫应答的标志性特征。
具体而言,烟雾暴露显著诱导γδT细胞高表达Il17a,并伴随着γ6δ4 T细胞这一优势克隆类型的明显扩增(图6a-d)。随着暴露时间延长,γ6δ4 T细胞持续发生克隆化扩增,并逐步获得典型的γδT17表型特征(图6e-g)。上述结果提示,克隆化扩增的γδT17细胞可能构成烟雾暴露相关免疫应答的标志性特征。
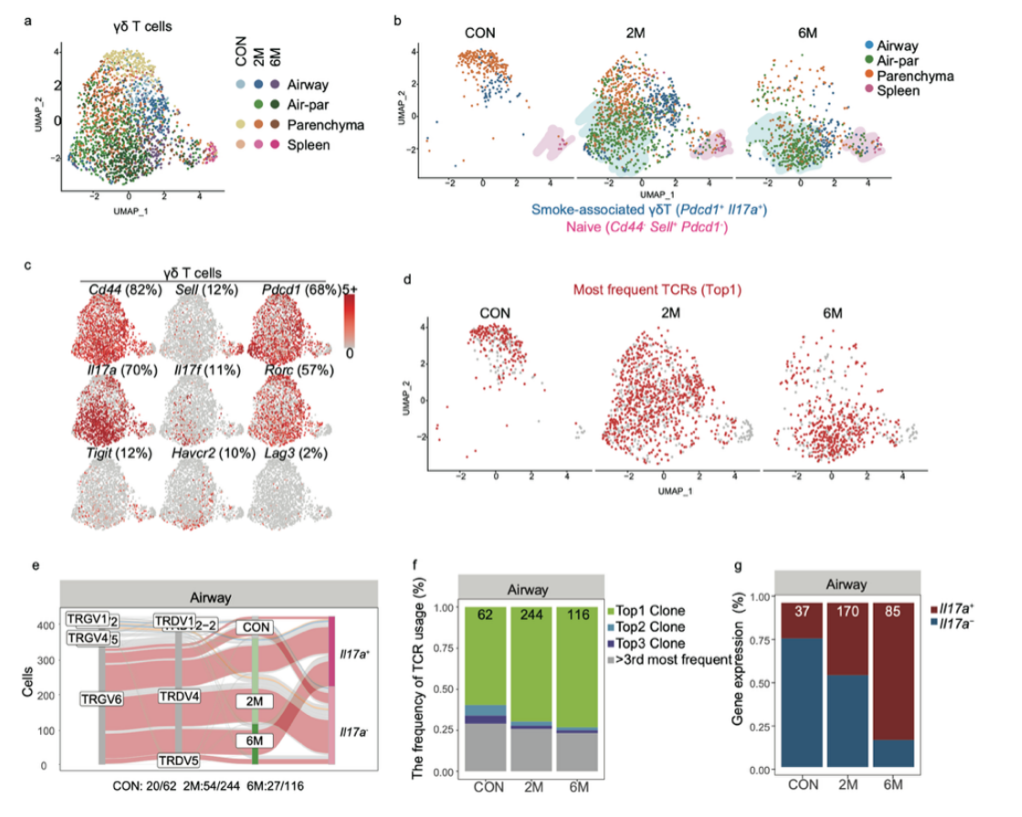
图6 烟草烟雾暴露对小鼠γδT细胞亚群的影响
为进一步解析烟雾暴露下γδT细胞的发育轨迹,研究团队利用RNA velocity和拟时序分析方法,对不同时间点、不同肺部解剖位点及脾脏中的γδT细胞进行了系统追踪。
分析结果显示,烟雾暴露可驱动不表达Il17a的γδT细胞沿单向轨迹逐步分化为表达Il17a的γδT17细胞,且该过程呈现出明显的时间依赖性(图7)。这一发现从动态发育层面证实了γδT细胞在烟雾刺激下向γδT17表型转变的趋势。
分析结果显示,烟雾暴露可驱动不表达Il17a的γδT细胞沿单向轨迹逐步分化为表达Il17a的γδT17细胞,且该过程呈现出明显的时间依赖性(图7)。这一发现从动态发育层面证实了γδT细胞在烟雾刺激下向γδT17表型转变的趋势。
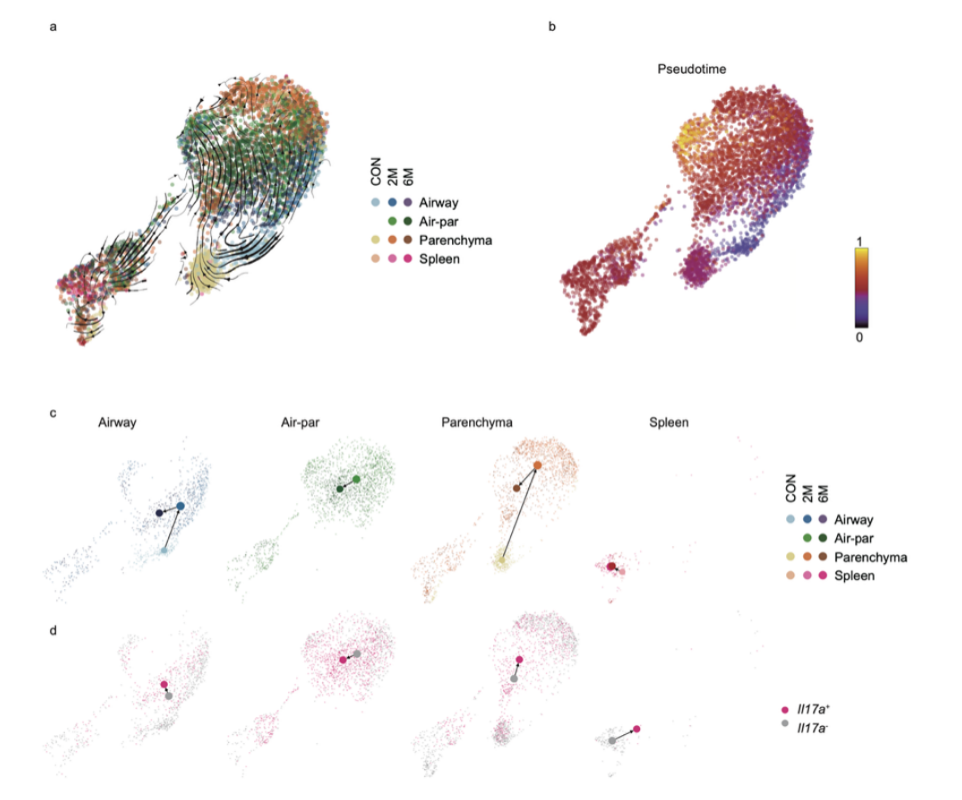
图7 烟草烟雾暴露驱动γδT细胞向γδT17细胞分化
γδT17细胞功能上具有保护作用
在功能学层面,研究团队通过体内动物实验进一步验证了γδT17细胞在烟雾诱导肺损伤中的作用。结果显示,敲除γδT细胞可显著加重气道炎症和肺气肿样病变,而回输体外扩增的γδT17细胞则可明显改善肺组织结构损伤和气流受限(图8)。这一结果表明,尽管γδT17细胞产生于炎症环境,但其在慢性烟雾暴露条件下具有重要的组织保护和修复潜力。
在功能学层面,研究团队通过体内动物实验进一步验证了γδT17细胞在烟雾诱导肺损伤中的作用。结果显示,敲除γδT细胞可显著加重气道炎症和肺气肿样病变,而回输体外扩增的γδT17细胞则可明显改善肺组织结构损伤和气流受限(图8)。这一结果表明,尽管γδT17细胞产生于炎症环境,但其在慢性烟雾暴露条件下具有重要的组织保护和修复潜力。
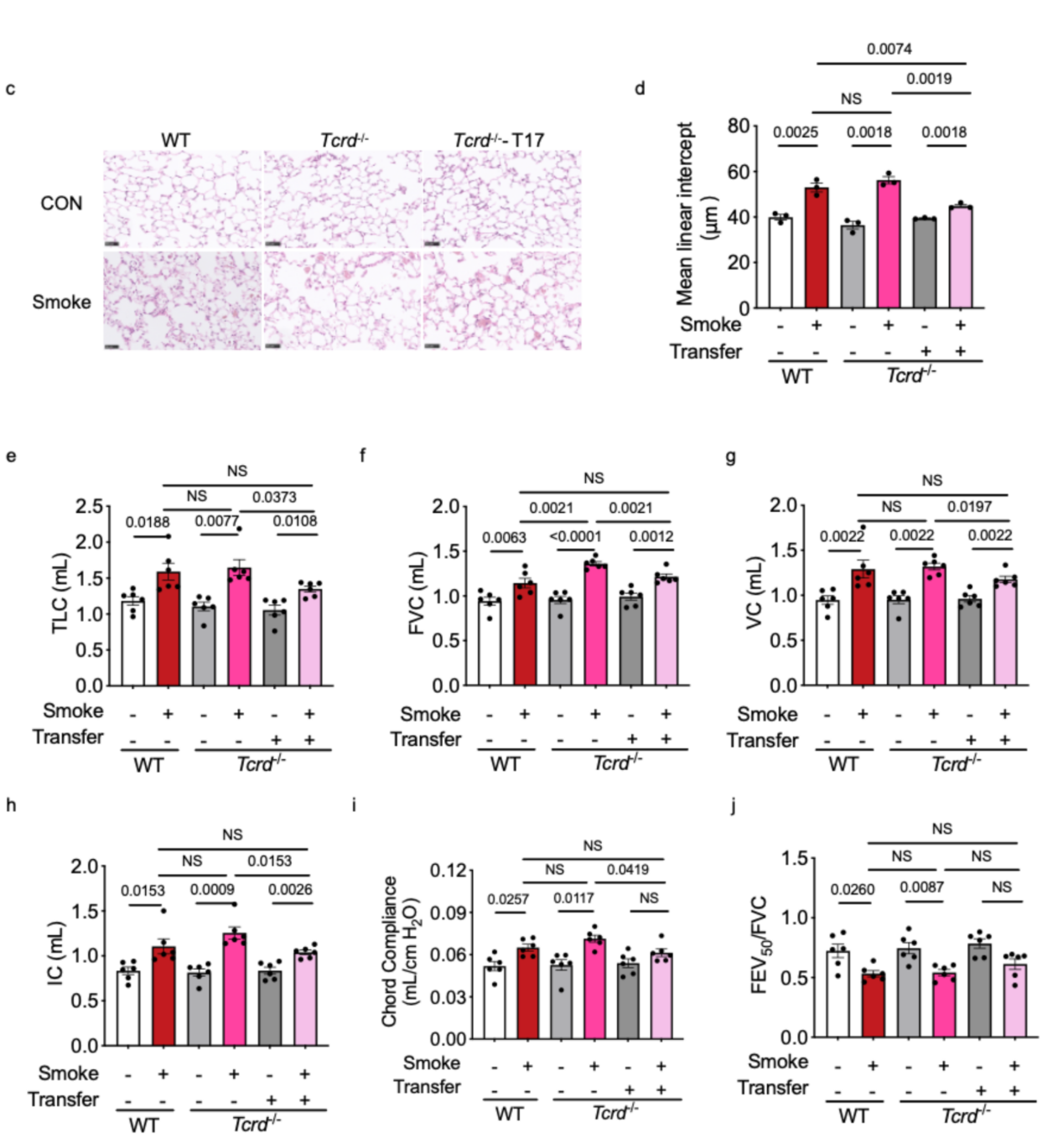
图8 γδT17细胞对气流受限及肺气肿样表型的改善作用
研究意义与展望
综上,该研究首次从单细胞和克隆水平系统描绘了烟草烟雾暴露诱导的T细胞免疫重塑图谱,明确了克隆化扩增的γδT17细胞在COPD发生发展中的关键作用。这一发现不仅深化了对COPD免疫炎症机制的理解,也为烟草烟雾诱导的免疫功能紊乱提供了潜在的早期诊断标志物和干预靶点。
未来,针对γδT17细胞的调控机制及其在不同疾病阶段中的功能异质性的深入研究,有望为COPD的早期预防和精准治疗提供新的思路和策略。
综上,该研究首次从单细胞和克隆水平系统描绘了烟草烟雾暴露诱导的T细胞免疫重塑图谱,明确了克隆化扩增的γδT17细胞在COPD发生发展中的关键作用。这一发现不仅深化了对COPD免疫炎症机制的理解,也为烟草烟雾诱导的免疫功能紊乱提供了潜在的早期诊断标志物和干预靶点。
未来,针对γδT17细胞的调控机制及其在不同疾病阶段中的功能异质性的深入研究,有望为COPD的早期预防和精准治疗提供新的思路和策略。






