胚胎发育是生命活动的基础,其中原肠运动阶段形成的外、中、内三个胚层,是所有器官形态建成的起点,内胚层更是肺、气管等呼吸器官的发育基础。长期以来,小鼠胚胎胚层发生的分子调控网络是发育生物学研究的重点与难点,而呼吸疾病的发生常与胚胎发育阶段的胚层分化、信号通路调控异常密切相关,解析这一过程的调控规律,对理解呼吸疾病的胚胎起源与发病机制至关重要。景乃禾团队此前已围绕小鼠原肠胚发育展开系列研究,构建了转录组与表观遗传全景图,发现了胚胎左-右体轴建立的新发育起点,为本次多组学整合研究奠定了坚实基础。
本研究中,团队利用10xmulti-omics双组学测序技术,精准解析了小鼠胚胎E6.5至E7.5阶段的单细胞基因表达与染色质开放特征,完成31种主要细胞类型的精准注释。在此基础上,团队开发出全新的基因组调控元件与表达基因连锁算法BioCRE,该算法在细胞类型特异性调控关系捕获、测序深度适应性、计算效率等方面均优于Signac、ArchR等主流工具,为解析基因调控网络提供了更高效的技术手段。基于BioCRE算法,团队首次将单细胞尺度的基因表达、染色质开放程度、转录因子与信号通路活性及响应性、细胞时空定位五维数据有机整合,成功绘制出小鼠原肠运动全过程的时空多组学调控网络图谱ST-MAGIC及升级版ST-MAGIC(+),构建了胚层谱系命运决定中关键分子调控机制的时序接力逻辑框架模型。
此外,研究团队发现,小鼠胚胎左-右体轴“早期不对称”阶段已存在调控元件的差异性开放模式,这一表观遗传“预先编程”特征,为理解左右肺发育不对称及相关呼吸疾病的发生机制提供了新的表观遗传视角;首次系统阐明了轴中内胚层谱系发育的“染色质-转录因子时序接力”规律,而轴中内胚层作为后续器官模式建成过程的组织者中心,其调控异常可能直接影响肺等呼吸器官的早期形成;明确了NODAL、WNT等经典信号通路的活性与染色质调控元件开放状态高度耦联,其“响应窗口”的时空精细调控规律,为解析这类信号通路异常引发的呼吸发育缺陷、肺部疾病提供了核心分子依据。同时,研究验证了NOTO、POU6F1等转录因子在结点细胞功能成熟及纤毛发生中的关键作用,而呼吸道纤毛功能异常正是多种先天性呼吸疾病、慢性气道疾病的重要病理特征。
在此基础上,研究还提出了谱系分化进程中的“多层级时空接力网络”调控框架,证实胚胎发育的分子调控是基因组非编码区、调控元件区整合信号通路、转录因子、表观遗传状态的跨模态协同作用过程,单纯的转录组或表观组研究难以全面解析其复杂机制。这一结论为呼吸疾病的研究提供了重要思路,提示需从多模态、多维度视角探究呼吸器官发育异常及相关疾病的分子机制。
呼吸系统的正常发育依赖于胚胎阶段胚层分化、基因调控、信号通路的精准时空调控,胚胎发育阶段的调控异常是先天性肺发育不全、支气管肺发育不良等先天性呼吸疾病,以及部分慢性阻塞性肺疾病、肺癌等后天性呼吸疾病的重要诱因。本次研究解析的胚胎发育核心调控规律、开发的新技术方法、构建的多组学调控网络框架,不仅为理解哺乳动物胚胎发育提供了全新的理论基础,更从胚胎源性角度为呼吸疾病的分子机制研究、潜在治疗靶点筛选、干细胞转化治疗研究提供了关键支撑。
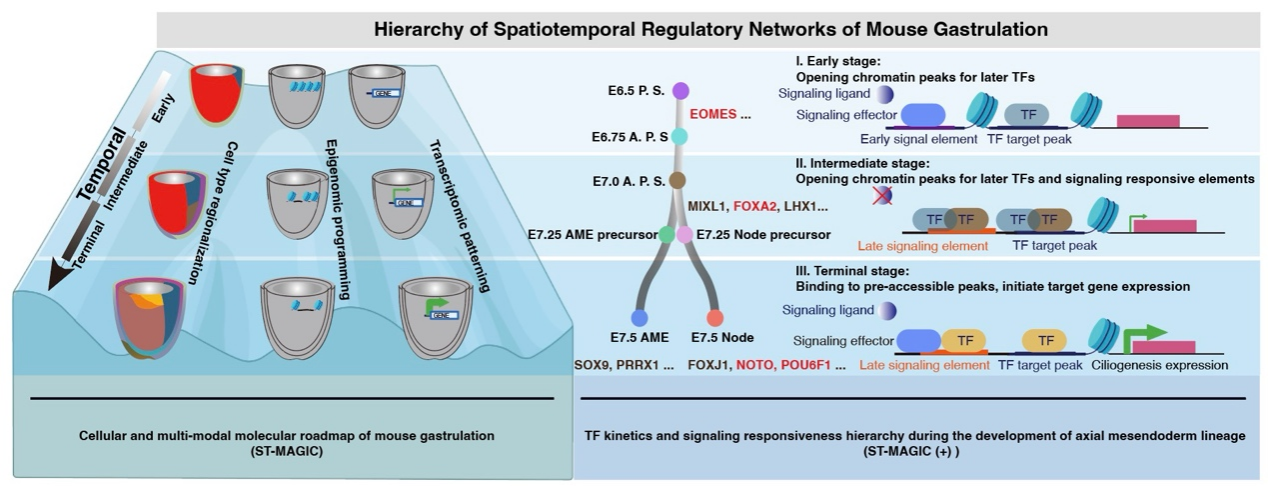
图1 小鼠胚胎原肠运动过程的时空调控网络模型
本研究由广州国家实验室景乃禾团队、索生宝团队合作完成,杨贤法副研究员、谢兵兵助理研究员、沈朋雷博士后、陈莹莹助理研究员为论文共同第一作者,景乃禾研究员、索生宝研究员为共同通讯作者。澳大利亚悉尼大学Patrick Tam教授、加拿大多伦多大学Chi-chung Hui教授为研究提供了重要指导与建议,广州国家实验室仪器支撑平台及动物中心等为项目推进提供了坚实的支撑作用。
原文链接:https://www.nature.com/articles/s41467-026-68291-w






