2026年1月7日,广州国家实验室/广州医科大学附属第一医院/呼吸疾病全国重点实验室丁彬彬-程璘令团队在Nature Communications发表题为O-GlcNAcylation of AMFR stabilizes TSPAN4 to regulate migrasome formation for viral release的研究论文,该研究聚焦病毒感染的分子传播机制,系统探索了病毒动态调控E3泛素连接酶AMFR的O-糖基化修饰,直接影响迁移体标志性蛋白四跨膜蛋白4(TSPAN4)稳定性,进而调控迁移体的生成以实现病毒胞间传播的新机制,为以病毒感染为核心的呼吸疾病防控提供了潜在靶点与理论支撑。
迁移体是细胞在运动过程中形成的一种细胞外细胞器,核心功能是释放mRNA、蛋白质、线粒体等细胞内物质介导细胞间通讯,近年已被证实在多种生理病理过程中发挥重要作用,如血管生成、缺血性脑损伤、增生性玻璃体视网膜病变等。而在呼吸疾病领域,病毒感染是引发急性呼吸道感染、肺炎等病症的核心诱因,最新研究提示迁移体可作为细胞外囊泡参与病毒释放,但该过程的分子调控机制仍不明确,极大限制了针对病毒源性呼吸疾病的靶向干预策略开发。TSPAN4作为迁移体的标志性蛋白,其介导的迁移体形成的调控机制及其在病毒感染性呼吸疾病中的病理功能,更是亟待破解的关键科学问题。
在本研究中,团队以RNA病毒VSV和DNA病毒HSV-1为研究模型,首先发现病毒可利用迁移体进行释放和传播,破坏迁移体形成可显著抑制病毒的释放。病毒颗粒可富集于迁移体中,这些含有病毒的迁移体可被邻近细胞摄取从而完成病毒胞间传播。进一步细致地探究发现,随着病毒感染时间增加,迁移体的数目出现先增加后减少的动态变化。
机制上,团队通过结合免疫共沉淀、蛋白质谱和siRNA筛选,揭示了调控迁移体形成的核心信号轴——内质网驻留E3泛素连接酶AMFR通过介导TSPAN4的泛素化促进其降解,从而抑制迁移体形成的负调控机制。进一步的探索发现O-糖基转移酶OGT介导AMFR第643位苏氨酸(Thr643)发生O-糖基化修饰,作为“分子开关”精确调控AMFR-TSPAN4信号轴,正调控迁移体的形成。体内co-IP和体外pull down结果表明,增强AMFR的O-糖基化可显著抑制其与TSPAN4的结合,进而稳定TSPAN4并促进迁移体的形成;而降低AMFR的O-糖基化则增强AMFR-TSPAN4互作和TSPAN4降解,导致迁移体无法形成。这一机制的发现,明确了迁移体生成的核心调控通路,为靶向干预病毒介导的呼吸疾病提供了关键分子靶点。
尤为值得关注的是,在病毒感染情况下,感染早期病毒通过上调AMFR的O-糖基化,抑制AMFR对TSPAN4的泛素化修饰及降解,增强迁移体形成,在子代病毒数量有限情况下利用迁移体进行有效胞间传播,同时逃避免疫识别;而在感染晚期,此时大量子代病毒已产生,迁移体介导的低效胞间传播反而限制病毒的扩散,病毒通过下调AMFR的O-GlcNAc糖基化,增强AMFR介导的TSPAN4降解,从而抑制迁移体形成,以适应病毒大规模释放的需求。
本研究揭示了病毒通过AMFR-TSPAN4信号轴调控迁移体形成从而利用迁移体进行传播的新策略,为呼吸疾病防控提出了全新干预思路。呼吸道病毒感染引发的肺炎、急性呼吸窘迫综合征等病症,始终是危害人类呼吸系统健康的重大公共卫生问题,而该研究明确的AMFR O-糖基化修饰、TSPAN4稳定性等关键调控节点,可作为开发新型抗病毒药物的潜在靶点——通过靶向调控迁移体形成,阻断病毒在呼吸道上皮细胞间的传播,为精准防控病毒源性呼吸疾病提供了重要理论基础与技术方向,有望推动呼吸疾病抗病毒治疗从广谱抑制向靶向干预升级。
迁移体是细胞在运动过程中形成的一种细胞外细胞器,核心功能是释放mRNA、蛋白质、线粒体等细胞内物质介导细胞间通讯,近年已被证实在多种生理病理过程中发挥重要作用,如血管生成、缺血性脑损伤、增生性玻璃体视网膜病变等。而在呼吸疾病领域,病毒感染是引发急性呼吸道感染、肺炎等病症的核心诱因,最新研究提示迁移体可作为细胞外囊泡参与病毒释放,但该过程的分子调控机制仍不明确,极大限制了针对病毒源性呼吸疾病的靶向干预策略开发。TSPAN4作为迁移体的标志性蛋白,其介导的迁移体形成的调控机制及其在病毒感染性呼吸疾病中的病理功能,更是亟待破解的关键科学问题。
在本研究中,团队以RNA病毒VSV和DNA病毒HSV-1为研究模型,首先发现病毒可利用迁移体进行释放和传播,破坏迁移体形成可显著抑制病毒的释放。病毒颗粒可富集于迁移体中,这些含有病毒的迁移体可被邻近细胞摄取从而完成病毒胞间传播。进一步细致地探究发现,随着病毒感染时间增加,迁移体的数目出现先增加后减少的动态变化。
机制上,团队通过结合免疫共沉淀、蛋白质谱和siRNA筛选,揭示了调控迁移体形成的核心信号轴——内质网驻留E3泛素连接酶AMFR通过介导TSPAN4的泛素化促进其降解,从而抑制迁移体形成的负调控机制。进一步的探索发现O-糖基转移酶OGT介导AMFR第643位苏氨酸(Thr643)发生O-糖基化修饰,作为“分子开关”精确调控AMFR-TSPAN4信号轴,正调控迁移体的形成。体内co-IP和体外pull down结果表明,增强AMFR的O-糖基化可显著抑制其与TSPAN4的结合,进而稳定TSPAN4并促进迁移体的形成;而降低AMFR的O-糖基化则增强AMFR-TSPAN4互作和TSPAN4降解,导致迁移体无法形成。这一机制的发现,明确了迁移体生成的核心调控通路,为靶向干预病毒介导的呼吸疾病提供了关键分子靶点。
尤为值得关注的是,在病毒感染情况下,感染早期病毒通过上调AMFR的O-糖基化,抑制AMFR对TSPAN4的泛素化修饰及降解,增强迁移体形成,在子代病毒数量有限情况下利用迁移体进行有效胞间传播,同时逃避免疫识别;而在感染晚期,此时大量子代病毒已产生,迁移体介导的低效胞间传播反而限制病毒的扩散,病毒通过下调AMFR的O-GlcNAc糖基化,增强AMFR介导的TSPAN4降解,从而抑制迁移体形成,以适应病毒大规模释放的需求。
本研究揭示了病毒通过AMFR-TSPAN4信号轴调控迁移体形成从而利用迁移体进行传播的新策略,为呼吸疾病防控提出了全新干预思路。呼吸道病毒感染引发的肺炎、急性呼吸窘迫综合征等病症,始终是危害人类呼吸系统健康的重大公共卫生问题,而该研究明确的AMFR O-糖基化修饰、TSPAN4稳定性等关键调控节点,可作为开发新型抗病毒药物的潜在靶点——通过靶向调控迁移体形成,阻断病毒在呼吸道上皮细胞间的传播,为精准防控病毒源性呼吸疾病提供了重要理论基础与技术方向,有望推动呼吸疾病抗病毒治疗从广谱抑制向靶向干预升级。
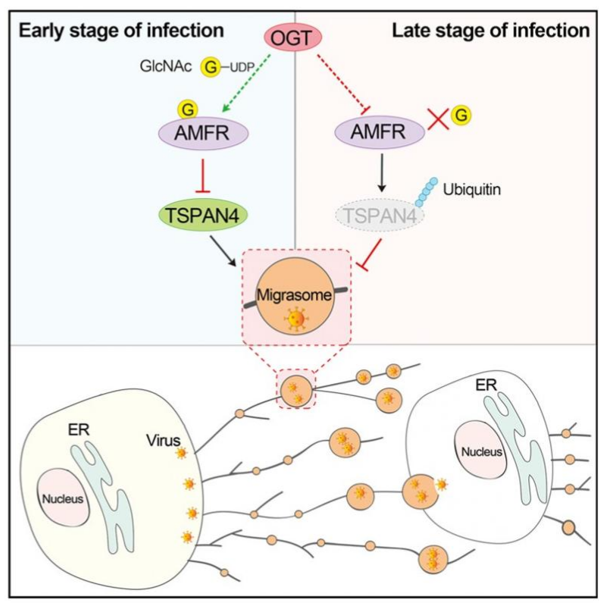
图1 病毒感染过程中,通过AMFRO-GlcNAc糖基化和TSPAN4泛素化修饰,动态调控迁移体形成的机制模型
广州国家实验室联合培养博士生余玲晖、李佳佳和美国加州理工学院韩依杨博士为本文共同第一作者,广州国家实验室/广州医科大学附属第一医院/呼吸疾病全国重点实验室丁彬彬研究员和程璘令教授为共同通讯作者。研究工作得到了广州国家实验室/广州医科大学赵金存教授、清华大学俞立教授、西安交通大学黄雨薇教授的大力支持和指导。
论文链接:https://doi.org/10.1038/s41467-025-68220-3





